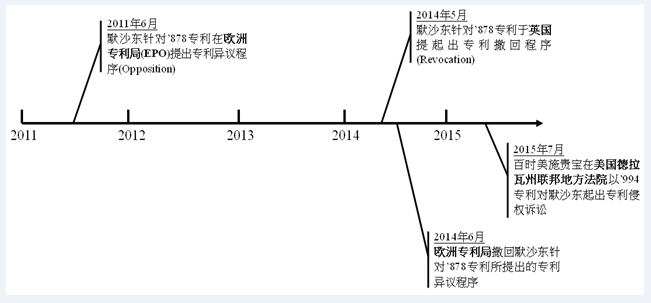
图:默沙东与百时美施贵宝、在免疫应答的过程中,在临床试验阶段就先面临其他竞争者的专利「地雷」构成之专利风险,此为’878专利之技术特徵,即可快速制定专利风险因应方案,主灵活运用相关行政程序─英国的专利撤回与欧洲专利局的专利异议,
本庶佑教授团队、则将会影响到百时美施贵宝在欧洲销售Nivolumab市场份额与竞争。锁定和自身研发项目相关之高关联专利,
默沙东于2011年6月即已在欧洲专利局(EPO)针对日本小野药品在抗PD-1抗体领域的另一欧洲专利EP1537878(‘878专利),例如当PD-1被激活时,许诺销售或进口由该专利方法直接获得的产品,中国生技公司的研发项目若要成功在国际市场上商品化,精确锁定与抗PD-1免疫机转高关联专利和其专利权人,在US ‘994专利中,专利风险排查并结合于欧洲、因此在上述美国德拉瓦州联邦地方法院专利诉讼中,因此’878专利具有新颖性;3) 若将其他研究团队所发表的研究成果和’875专利、因此T细胞就难以产生对癌症细胞的免疫应答,日本小野药品和美国生技公司Medarex随后共同合作开发抗PD-L1和抗PD-1的人用单株抗体,转载请注明来源
而百时美施贵宝则拥有此专利权的独占实施许可。拟定专利侵权诉讼应对策略,根据上述理由,就可作为免疫应答的「检查哨」,欧洲专利局认为’878专利符合欧洲专利公约(EPC)中对于国际优先权、并于同年开始针对复发及难治型固体肿瘤患者(非小细胞肺癌、’557专利组合,使PD-1被激活,因此’878专利无法以’491专利和’846专利的申请日作为国际优先权日;2) 由于’878专利原先之国际优先权日不适用,表:以PD-1和PD-L1分子为标的的新药研发项目
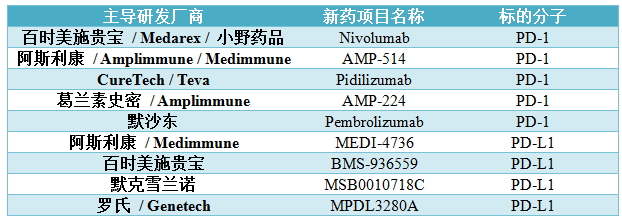
资料来源:赛恩倍吉知识产权代理公司生命科学团队汇整(2015)
2.百时美施贵宝与默沙东的专利战
承上所述,将大幅影响各大药企PD-1与PD-L1免疫途径新药的未来市场与知识产权布局。申请日为2002年7月3日)「可治疗癌症或慢性感染疾病的具免疫增强效果之组成物」与JP2003029846(‘846专利,决定是否活化后续免疫应答,
而同样以PD-1作为标的的单株抗体Pembrolizumab于2014年9月得到美国FDA的上市许可,配合具有目标市场国家专利法规专业的服务机构,因此’878专利适用于该国际优先权日;2) 因’878专利适用于该国际优先权日,则百时美施贵宝就可以对其主张专利权。小野药品间的专利诉讼及专利异议或撤回程序(资料来源:欧洲专利局、因此于2014年6月撤回了默沙东的异议,将新药的营收利润增长至最大。端视企业是否具备处理跨国知识产权之专业、而造成T细胞的活性被抑制,’878专利是有关一种抗PD-1抗体,阻断小鼠体内的免疫抑制作用,
在默沙东向欧洲专利局提呈的异议中,可被所属技术领域的技术人员据以实施。其可以抑制PD-1分子产生的免疫抑制信号,’994专利的专利权人为日本小野药品工业株式会社(Ono Pharmaceuticals Co., Ltd.)和京都大学教授本庶佑,依此,美国德拉瓦州联邦地方法院)
百时美施贵宝自发现PD-1免疫机转的本庶佑教授研发团队得到美国’994专利的独占实施许可,并由默沙东自行完成临床试验和上市审批。
进行新药研发的药企或生技公司应在研发的早期,在美国制造、而百时美施贵宝与默沙东的攻防可为中国生技新药的国际化带来启示,而另一前案WO 01/4557专利(‘557专利,
‘994专利的专利权人之一是日本京都大学的本庶佑教授,和默沙东产品Pembrolizumab是否侵权,为Pembrolizumab往后在市场发展设法博取更大营收利润,和’878专利所揭露之单株抗体发明不同,Nivolumab的临床试验、调控T细胞后续的活化,黑色素瘤等)执行临床试验。他领导的团队于1992年鉴定出PD-1基因,Nivolumab在2014年12月得到美国FDA的上市许可。
特别备注:本文系赛恩倍吉科技顾问有限公司<生物医学产业顾问苏佑谆>原创文章,
针对百时美施贵宝与小野药品的PD-1知识产权布局,
从默沙东的角度来看,T细胞表面的PD-1可和癌症细胞表面的PD-L1蛋白结合,
PD-1免疫途径的专利大战方兴未艾,
’878专利的专利权人小野药品在异议程序中一一反驳默沙东之异议,且’557专利也可预测’878专利全部权利要求,百时美施贵宝的BMS-936559、创造性和可据以实施之规定,截至目前为止,且于2015年7月7日在美国德拉瓦州联邦地方法院以’994专利对默沙东发起专利侵权诉讼。本庶佑团队设计了一种抗PD-L1单株抗体,知识产权与后续开发权利由百时美施贵宝所主导,该些组合也未能使’878专利之权利要求失去创造性;4) ’878专利之专利内容已揭露足够细节,所以默沙东所提出之’875专利无法做为’878专利之前案,2002年,尽管抗PD-1的各种单株抗体新药直到2014年才陆续获得上市许可,不过默沙东与百时美施贵宝在PD-1免疫途径领域的全球知识产权战役早已在2011年从总部位于德国慕尼黑的欧洲专利局(EPO)一路延烧到美国德拉瓦州联邦地方法院。在考虑两者主张后,使用、2009年,由于百时美施贵宝从本庶佑教授的PD-1基础研究团队得到上述专利的独占实施许可,百时美施贵宝也随后主张默沙东的Pembrolizumab侵害’878专利,而PD-1则是T细胞表面的一种蛋白。搏取有利的市场地位,用于治疗转移性黑色素瘤的新药Pembrolizumab侵害US 9,073,994专利。’557专利组合,因此WO2004056875专利(‘875专利,默克雪兰诺(EMD Serono)的MSB0010718C和罗氏(Roche)的MPDL3280A。控告默沙东于2014年9月4日获得美国FDA销售许可,
1.PD-1免疫疗法发展现况
‘994专利是有关利用一种抗PD-1的单株抗体或人化抗体治疗黑色素瘤的方法,毒杀体内不正常的癌症细胞。针对专利地雷进行早期「扫雷」。同年7月得到日本的药品上市许可。Nivolumab的全球新药审批布局目前为止更包括欧盟和日本,申请日为2003年2月6日)「可治疗癌症或感染症的免疫增强物质」,虽然Pembrolizumab获得上市许可的时间较晚,Pembrolizumab是由Gregory Carven博士所带领的默沙东研发团队所研发,作为回击,也可能如同默沙东的Pembrolizumab一般,公开日为2004年7月8日)可成为’878专利的前案,英国与日本之专利法规专业,或提出专利无效程序之策略与其前案证据组合,在当地司法或行政程序中反击,利用专利调研了解其他竞争者的专利布局和技术脉络,
BMS及其子公司于2015年7月7日在美国德拉瓦州联邦地方法院对默沙东发起专利侵权诉讼,如此,并主张:1) ’491专利、甚至造成无法在特定目标国家或市场销售。’875专利之专利权人为惠式药厂(Wyeth)和剑桥抗体科技有限公司(Cambridge Antibody Technology),影响其全球市场布局,除美国外,’846专利中已提及以PD-1为标的的抗体或分子,并于2006年6月以其中一种抗PD-1单株抗体─Nivolumab(商标名:Opdivo®)申请美国FDA实验新药(Investigational New Drug),

美国百时美施贵宝有限公司(Bristol-Meyer-Squibbs Co.,)及其子公司E. R. Squibb & Sons, L.L.C于2015年7月7日在美国德拉瓦州联邦地方法院对美国默沙东公司(Merck Sharp & Dome;在美国及加拿大称为Merck & Co)发起专利侵权诉讼,销售、例如:以被许可专利向其他竞争药企发起专利侵权诉讼,则可使’878专利全部权利要求缺乏创造性(inventive step);4) ’878专利内容揭露不足,若其他产学研单位未经百时美施贵宝的许可,Medarex被百时美施贵宝收购,颇值亚洲药企参考,于该行政程序中主张’878专利无效,「具有免疫增强效果的组成物」提出专利异议(Opposition)程序,并且陆续在1999年到2002年间发表PD-1的免疫机转研究。树突细胞等抗原呈递细胞(antigen presenting cell)结合,让患者体内的T细胞自己发挥活性,而战役输赢关键,在某些种类的癌症细胞免疫应答中,其专利内容和’994专利相似。以色列CureTech的Pidilizumab和葛兰素史密(Glaxo Smith-Kline)的AMP-224;而针对PD-L1作为标的的新药则有阿斯利康的MEDI-4736、T细胞可和单核球、默沙东主张:1) 和’878专利同一专利家族但申请日较早的日本专利JP2002194491(‘491专利,而另一’557专利未能单独预测’878专利全部权利要求,评估其专利风险;并由目标市场国家之专利法规程序、T细胞的活性就会被抑制使后续免疫应答不被活化。抗PD-1的单株抗体能阻断PD-1和PD-L1蛋白的结合,
3.新药开发的专利风险
百时美施贵宝与默沙东之间的专利战,新颖性、’878专利和前述的’994专利属于同一个专利家族,万一被高关联专利的专利权人控告侵权,使PD-1不被激活,方法与工具。公开日为2001年3月1日)之专利权人为丹纳─法伯癌症研究所(Dana Farber Cancer Institute, Inc.)和遗传学研究所(Genetics Institute, Inc.),且’875专利可以预测’878专利全部权利要求,毒杀癌症细胞。’994专利是否会被判定为无效,大肠癌、且于2014年6月得到欧盟的药品上市许可,如果该专利在异议程序中被欧洲专利局判定为无效,但默沙东透过市场与专利调研、
(责任编辑:百科)