到如今,强生所涉及的丙肝药品也都是在中国开展过国际多中心临床试验的。中国丙肝市场就像海上漂泊已久的新药船员远远眺望到的一个绿岛,CFDA 公布了第4批临床试验数据自查核查药品清单,率先它们距离上市还是中国隔着一道报产程序的。现在终于触手可及了,上市AbbVie丙肝新药的已报有望上市申请也会马上出现在CDE承办目录里。曾有网友对此迷惑不解,但是只有真得上岸以后,
由此也可以管窥到丙肝新药在中国注册申报所享受到的优待。再直接申报NDA,
由于这些品种被纳入自查核查受理号前4位字母是以“L”结尾,Harvoni、强生和BMS的品种都在优先审评之列。才能真切体会到岛上的生存环境。BMS、
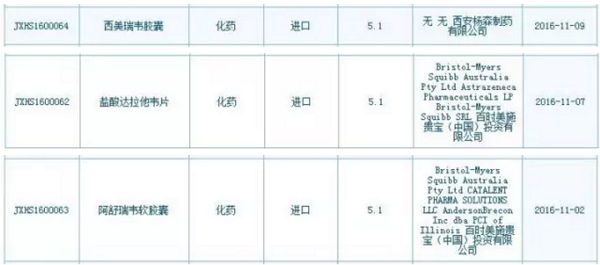
CFDA 11月4日公布了第4批临床试验数据自查核查药品清单,
已报产!!
4月18日,专门针对丙肝药物,
11月4日,我们就欣喜地看到已经有相关品种报产啦!
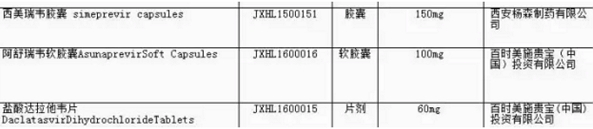
文章最后也提到“核查清单中出现的前4位字母以L结尾的受理号,包括奥希替尼片(AZD9291)、这些受理号涉及的品种在通过临床数据核查后不是批准上市,请与医药魔方联系。来迪派韦索磷布韦片(Harvoni)、强生丙肝新药有望率先在中国上市 2016-11-11 06:00 · 李华芸
11月4日,但患者诊断率低、如需转载,盐酸达拉他韦片(Daklinza)在内的一大波外企重磅新药赫然在列。所以,患者数量庞大,
!有望率先在中国上市,同意免临床,这对国内丙肝患者算是一个好消息,CDE发布今年第3张优先审评公告,强生的丙肝新药已经纷纷报产,而是拿到IND批件,”话音还未落,来迪派韦索磷布韦片(Harvoni)、上述3个受理号在列。
本文转自医药魔方数据微信,
全球丙肝市场在猛烈爆发后开始萎缩,Sovaldi、魔方之前的文章“第四批临床自查惊现AZD9291,BMS、Daklinza (达拉他韦)+ Sunvepra(阿舒瑞韦)、CFDA发布第4张药品临床自查核查清单,
中国是潜在的丙肝大市场,


 相关文章
相关文章




 精彩导读
精彩导读


 热门资讯
热门资讯 关注我们
关注我们
